傳統的(de)無菌标本的(de)培養是病原診斷的(de)“金(jīn)标準”[1,2],但(dàn)其診斷的(de)敏感性遠不能(néng)達到(dào)臨床病原診斷的(de)需求。宏基因組新一代測序技術(shù)(mNGS)相(xiàng)比較傳統方法,具有(yǒu)快速,靈敏度高(gāo)的(de)優勢,可(kě)以同時檢測出一大(dà)群差異極大(dà)的(de)微生物(wù)類群,尤其可(kě)以無差别的(de)檢測出已知或未知病原和(hé)耐藥性基因信息[3,4],顯著提升臨床病原診療效能(néng)。有(yǒu)學者預測在未來10年内,宏基因組測序将作爲常規檢測手段應用(yòng)于對病原體診療方面[5]。
在上(shàng)篇中,我們已經詳細介紹了“宏基因組學發展簡史”和(hé)mNGS檢測前注意事項,在本篇,我們将接著(zhe)介紹mNGS檢測後的(de)注意事項。
mNGS檢測後注意事項
一、mNGS檢測影響因素[6]
1. 病原體基因組大(dà)小(xiǎo)

2. 病原體生物(wù)結構

3. 樣本人(rén)源占比

二、mNGS報告解讀(dú)
1. 微生物(wù)菌種類型
明(míng)确的(de)緻病菌(低序列也(yě)需要臨床考慮):
結核分(fēn)枝杆菌複合群、鳥分(fēn)枝杆菌、胞内分(fēn)枝杆菌、膿腫分(fēn)枝杆菌、軍團菌、諾卡菌、流感病毒、新冠病毒、曲黴、新型隐球菌、馬爾尼菲藍狀菌、組織胞漿菌、腺病毒、耶氏肺孢子菌、鹦鹉熱(rè)衣原體、肺炎支原體、呼吸道合胞病毒等等。
條件(jiàn)緻病菌(結合标本類型、序列數、微生物(wù)排名、動态變化及臨床診斷綜合判斷):
銅綠(lǜ)假單胞菌、鮑曼不動杆菌、肺炎克雷伯菌、肺炎鏈球菌、屎腸球菌、糞腸球菌、念珠菌、流感嗜血杆菌、嗜麥芽假單胞菌等等[6]。
常見的(de)定植菌:
(1)呼吸道:丙酸杆菌屬、棒狀杆菌屬、葡萄球菌屬、莫拉菌屬、韋榮球菌屬、鏈球菌屬、嗜血杆菌屬、梭杆菌屬、奈瑟菌屬、普雷沃菌、假單胞菌屬、卟啉單胞菌屬等;
(2)皮膚:結核硬脂酸棒狀杆菌、頭狀葡萄球菌、表皮葡萄球菌、模仿棒狀杆菌、藤黃(huáng)微球菌、痤瘡丙酸杆菌、人(rén)葡萄球菌、非發酵棒狀杆菌、緩症鏈球菌、球形馬拉色菌、限制(zhì)馬拉色菌、合軸馬拉色菌、塔賓曲黴等。
2. 陽性标準(僅供參考)
腦(nǎo)脊液樣本:
(1)對于細菌、真菌與寄生蟲,RPM(指每百萬序列的(de)特異性讀(dú)長比率,RPM=RPM 腦(nǎo)脊液/RPM 非模闆對照(zhào))≥10,判斷爲陽性;
(2)對于病毒(DNA或RNA病毒),檢出讀(dú)長應至少(shǎo)覆蓋全基因組的(de) 3 個(gè)非重疊區域,判斷爲陽性[7]。
呼吸道樣本:
(1)細菌(分(fēn)枝杆菌除外)、真菌、病毒:病原種類的(de)相(xiàng)對豐度>30%,或某一病原培養陽性且mNGS序列數>50;
(2)結核分(fēn)枝杆菌:隻要有(yǒu)一條序列即可(kě)判斷陽性;
(3)有(yǒu)臨床其他(tā)試驗(病理(lǐ)、培養、塗片、抗原或抗體檢測、PCR)證明(míng)某 一微生物(wù)陽性時,mNGS鑒定的(de)該微生物(wù)被歸類爲确認病原體;
(4)如(rú)果僅有(yǒu)mNGS檢測出的(de)傳染性病原體,而沒有(yǒu)其他(tā)任何臨床試驗驗證,則此微生物(wù)被認爲是潛在的(de)病原體。所有(yǒu)經mNGS鑒定檢出但(dàn)不符合mNGS 陽性結果标準的(de)微生物(wù)都(dōu)被認爲是不确定病原體[8-10]。
血液樣本:
(1)明(míng)确感染(definite):mNGS檢測的(de)病原結果與其他(tā)微生物(wù)檢測方法結果一緻(同一樣本檢測期限爲7天);
(2)臨床診斷(probable):根據臨床、放(fàng)射學或實驗室檢查結果,測序病原體結果被認爲是膿毒症預警的(de)可(kě)能(néng)原因;
(3)拟診(possible):病原結果具有(yǒu)與臨床表現一緻的(de)潛在緻病性,但(dàn)對症狀的(de)另一種解釋更有(yǒu)可(kě)能(néng);
(4)不大(dà)可(kě)能(néng)(unlikly):結果與臨床表現不一緻[11]。
共識(阈值):
(1)一般細菌:mNGS檢測到(dào)某種細菌(種水(shuǐ)平)的(de)序列數是其餘所有(yǒu)細菌的(de)10倍以上(shàng),有(yǒu)臨床意義;
(2)真菌:mNGS檢測到(dào)真菌(種水(shuǐ)平)的(de)序列數是其餘所有(yǒu)真菌的(de)5倍以上(shàng),有(yǒu)臨床意義;
(3)MTB:爲明(míng)确緻病菌,環境污染的(de)可(kě)能(néng)小(xiǎo)。此外,因MTB爲胞内緻病菌,細胞外遊離(lí)DNA 少(shǎo),且MTB核酸提取效率低,mNGS隻要檢測到(dào)1條屬水(shuǐ)平的(de)MTB複合群序列,且能(néng)排除其他(tā)标本攜帶污染,就有(yǒu)臨床意義;
(4)非結核分(fēn)枝杆菌:可(kě)能(néng)是環境中污染菌,若檢出, 需結合背景微生物(wù)庫和(hé)mNGS原始細菌列表進行(xíng)結果判讀(dú)。若排除污染後屬水(shuǐ)平或種水(shuǐ)平序列數排名前十,則有(yǒu)臨床意義[12]。
3. 報告解讀(dú)常見錯誤
(1)Reads數最大(dà),不一定是緻病病原體:
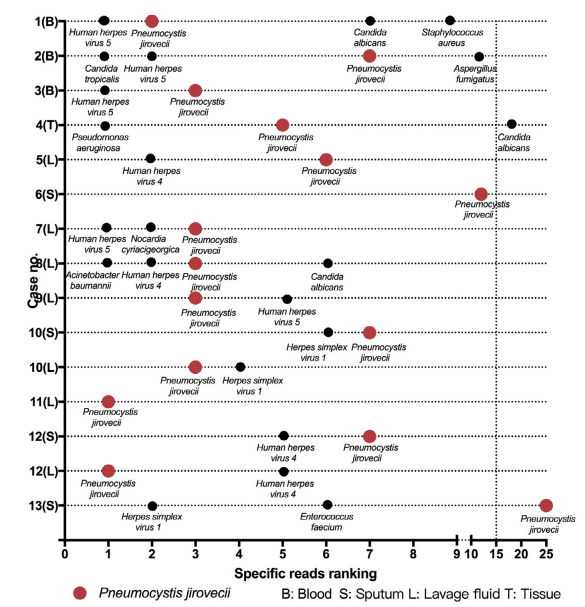
一項在13例耶氏肺孢子(PJP)感染病例中,mNGS檢出的(de)病原體reads數排名顯示,PJP不都(dōu)是排名第一,但(dàn)是确是緻病病原體。所以,mNGS檢出病原體reads數的(de)大(dà)小(xiǎo)不一定決定緻病的(de)情況[7]。
(2)“被扔掉的(de)數據”,不一定沒有(yǒu)用(yòng)(病例源自微信公衆号“呼吸界”):

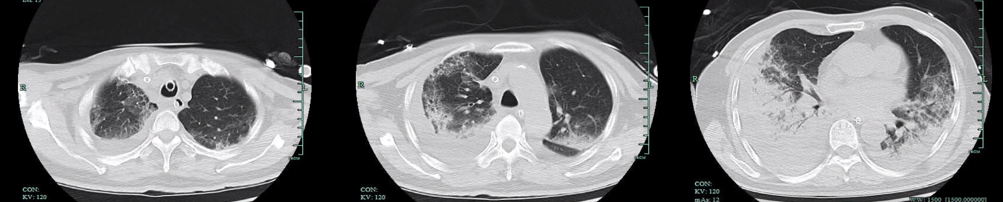

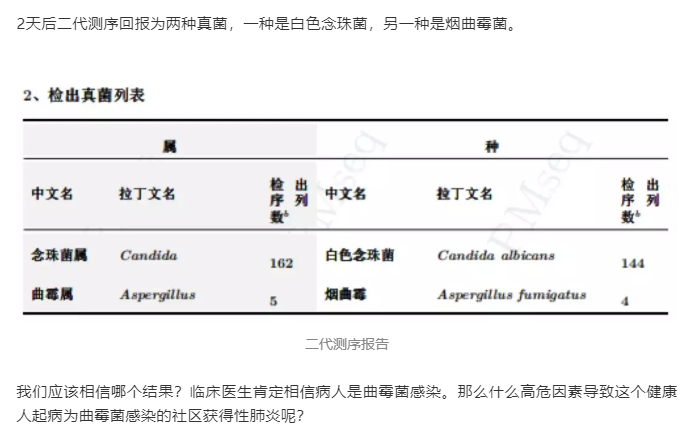
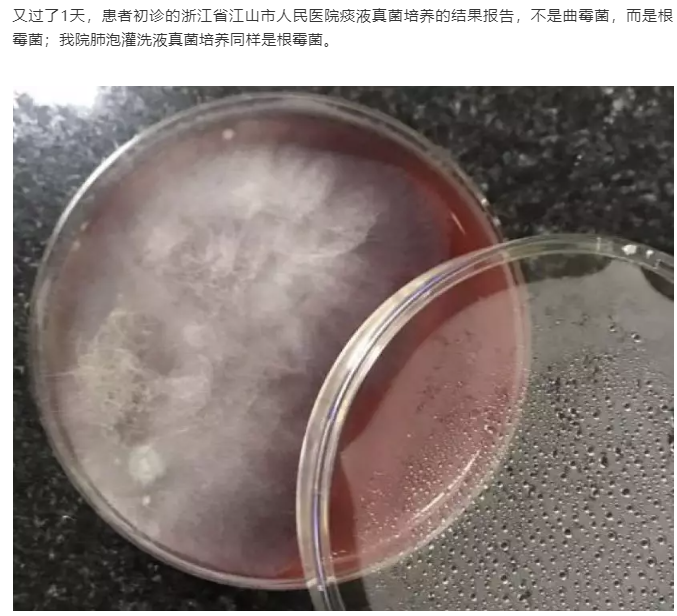
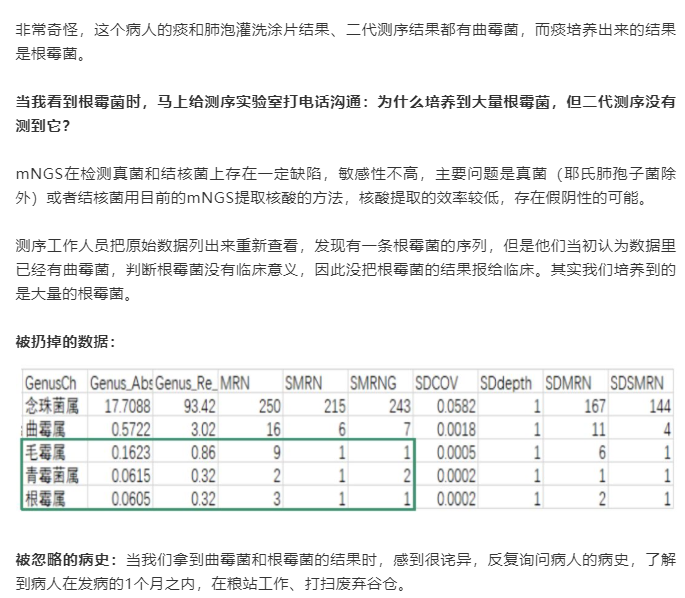
因此,在報告解讀(dú)時,需要注意檢出的(de)疑似微生物(wù)列表,因爲這也(yě)可(kě)能(néng)就是導緻病人(rén)緻病的(de)主要原因。
(3)“不常見”的(de)菌,不一定沒有(yǒu)意義(病例源自微信公衆号“呼吸界”):

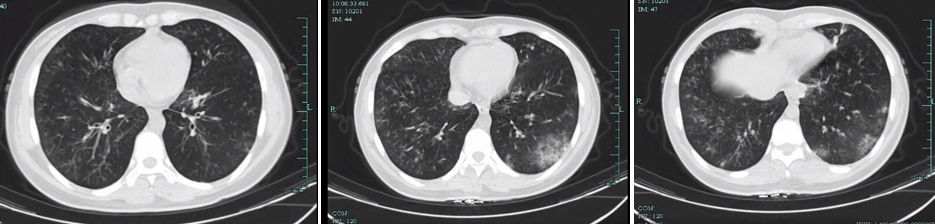
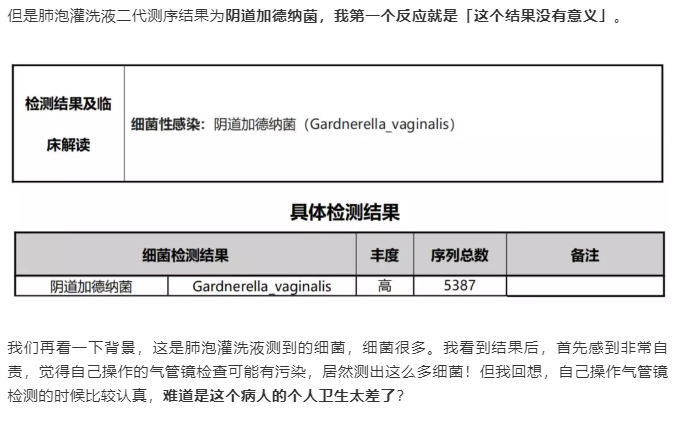
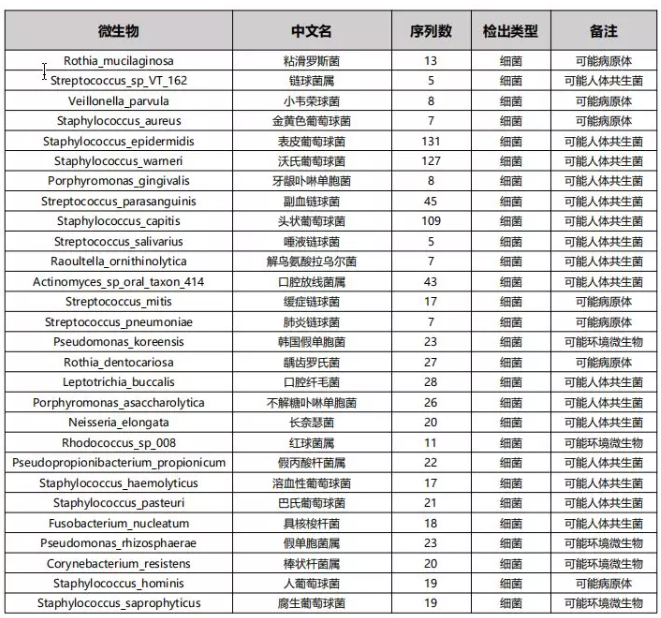

結論:這個(gè)病人(rén)爲女(nǚ)性同性戀,所以,我們在遇到(dào)部位 “不常見” 病原檢出時,一定要大(dà)膽實踐,小(xiǎo)心求證。
總結:
(1)mNGS已經越來越多的(de)被臨床所熟知,我們臨床醫生需要對其做好一定的(de)了解,才能(néng)更好的(de)利用(yòng)好這個(gè)工(gōng)具,更好的(de)幫助臨床;
(2)mNGS檢測前(樣本類型及采集等)和(hé)檢測後(報告解讀(dú))是我們臨床醫生可(kě)控部分(fēn),盡可(kě)能(néng)的(de)去遵循“專家共識”,讓mNGS檢測更有(yǒu)意義;
(3)目前mNGS尚無公認的(de)陽性阈值标準,在一定情況下,我們可(kě)以用(yòng)已發表的(de)文(wén)獻數據作一定的(de)參考;
(4)感染性疾病病原診斷要以患者爲中心,臨床起主導作用(yòng),最終還是要回到(dào)患者本身。所以,面對mNGS技術(shù),我們臨床要大(dà)膽的(de)實踐,小(xiǎo)心的(de)求證。
[1]甯永忠. 細菌性感染性疾病的(de)診斷分(fēn)級. 中華傳染病雜志, 2015, 33(1): 49-52.
[2]Donnelly JP, Chen S, Kauffman C, et al. Revision and Update of the Consensus Definitions of Invasive Fungal Disease From the European Organization for Research and Treatment of Cancer and the Mycoses Study Group Education and Research Consortium. Clinical Infectious Diseases, 2020, 71(6):1367-1376.
[3]Carpenter ML, Tan SK, Watson T, et al. Metagenomic Next-Generation Sequencing for Identification and Quantitation of Transplant-Related DNA Viruses. Journal of clinical microbiology, 2019, 57(12): e01113-19.
[4]Couto N, Schuele L, Raangs EC, et al. Critical steps in clinical shotgun metagenomics for the concomitant detection and typing of microbial pathogens. Scientific reports, 2018, 8(1):13767.
[5]Forbes JD, Knox NC, Ronholm J, et al. Metagenomics: The Next CultureIndependent Game Changer. Frontiers in microbiology, 2017, 8:1069.
[6]戴媛媛;馬筱玲. 宏基因組二代測序技術(shù)在臨床病原學診斷中的(de)應用(yòng). 臨床檢驗雜志, 2021.39(1):3.
[7]Miller Steve; Naccache Samia N; Samayoa Erik, et al. Laboratory validation of a clinical metagenomic sequencing assay for pathogen detection in cerebrospinal fluid. Genome research, 2019.29(5):831-842.
[8]Chen YQ, Feng W, Ye K, et al. Application of Metagenomic Next-Generation Sequencing in the Diagnosis of Pulmonary Infectious Pathogens From Bronchoalveolar Lavage Samples. Front Cell Infect Microbiol, 2021, 11:541092. 24.
[9]Li H, Gao H, Meng H, et al. Detection of pulmonary infectious pathogens from lung biopsy tissues by metagenomic next-generation sequencing. Front Cell Infect Microbiol, 2018, 8:205. 25.
[10]Langelier C, Zinter MS, Kalantar K, et al. Metagenomic sequencing detects respiratory pathogens in hematopoietic cellular transplant patients. Am J Respir Crit Care Med, 2018, 197:524–528.
[11]Blauwkamp TA, Thair S, Rosen MJ, et al. Analytical and clinical validation of a microbial cell-free DNA sequencing test for infectious disease. Nat Microbiol, 2019, 4(4): 663-674.
[12]Yi Zhang; Jing-Wen Ai; Peng Cui; et al. A cluster of cases of pneumocystis pneumonia identi