細菌耐藥性可(kě)分(fēn)爲天然耐藥性和(hé)獲得耐藥性,各種細菌的(de)耐藥機制(zhì)各有(yǒu)不同,但(dàn)主要有(yǒu)産生滅活酶或鈍化酶,藥物(wù)作用(yòng)靶位的(de)變化,細胞壁通透性改變,主動外排機制(zhì)等。隻有(yǒu)了解這些機理(lǐ)才能(néng)更好地(dì)防止細菌産生耐藥性。
一、細菌耐藥性的(de)産生及分(fēn)類
1. 細菌耐藥性的(de)産生
細菌耐藥性又(yòu)稱抗藥性,是指細菌與抗菌藥物(wù)多次接觸後,對藥物(wù)的(de)敏感性下降或消失。耐藥性一旦産生,藥物(wù)的(de)化學治療作用(yòng)就明(míng)顯下降。
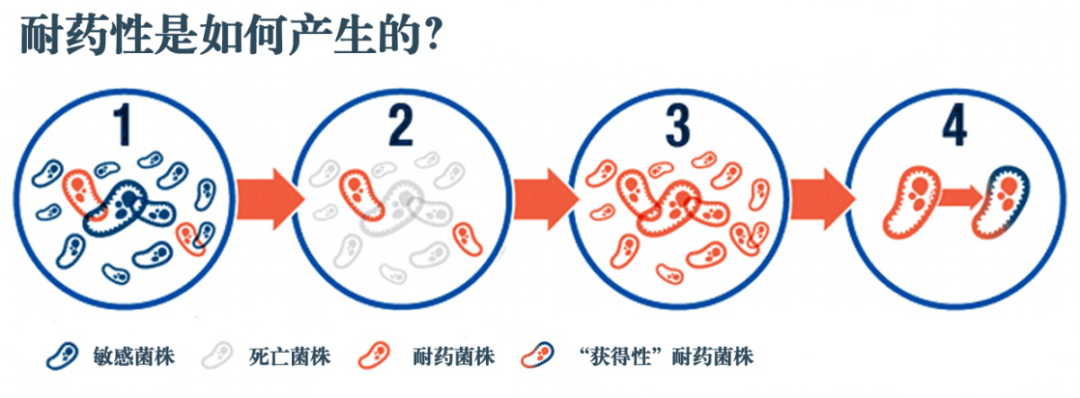
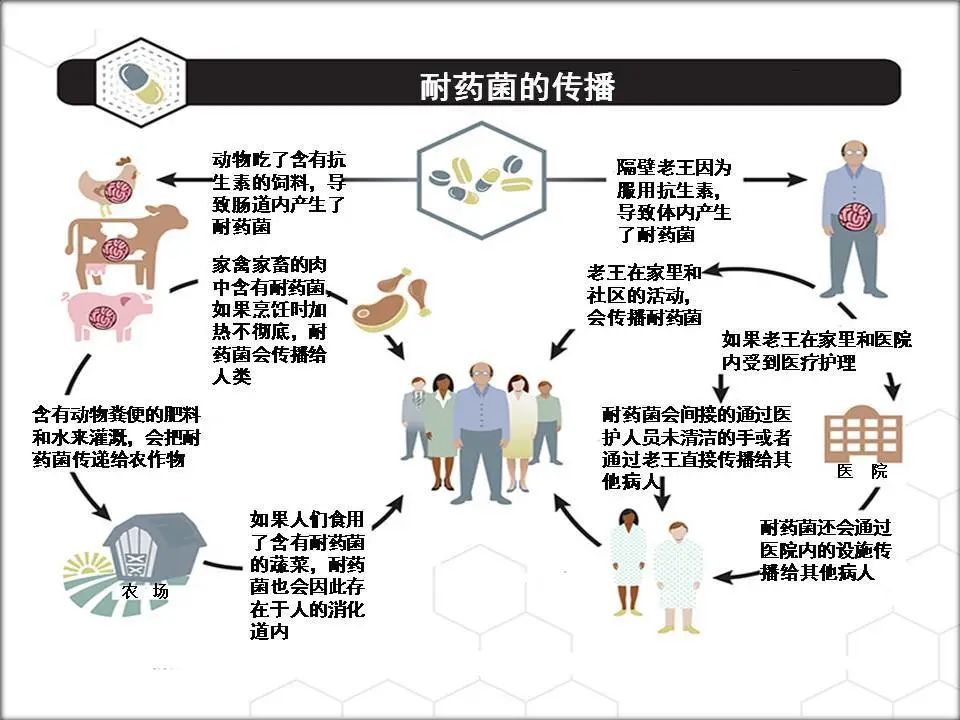
2. 細菌耐藥性的(de)種類
(1)天然耐藥性
天然耐藥性又(yòu)稱固有(yǒu)耐藥性,是由染色體遺傳基因介導的(de)耐藥性,它代代相(xiàng)傳不會(huì)改變。如(rú)鏈球菌對氨基糖苷類抗生素天然耐藥;腸道革蘭氏陰性杆菌對青黴素天然耐藥;銅綠(lǜ)假單胞菌對多數抗生素均不敏感。
(2)獲得耐藥性
獲得耐藥性是由于細菌與抗生素接觸後,由質粒介導,通過改變自身的(de)代謝途徑,使其不被抗生素殺滅,而且質粒所帶的(de)耐藥基因易于傳播,耐藥菌迅速生長繁殖。比如(rú)金(jīn)黃(huáng)色葡萄球菌産生 β-内酰胺酶類抗生素耐藥。
細菌的(de)獲得性耐藥可(kě)因不再接觸抗生素而消失,也(yě)可(kě)由質粒将耐藥基因轉移至染色體而代代相(xiàng)傳,成爲天然耐藥。
二、耐藥性的(de)産生機制(zhì)
1. 細菌産生破壞抗生素結構的(de)酶
細菌爲了生存,可(kě)以産生一種或多種水(shuǐ)解酶或鈍化酶來水(shuǐ)解或修飾進入細菌細胞内的(de)抗生素,使之失去生物(wù)活性,這也(yě)是目前引起細菌耐藥性的(de)最重要機制(zhì)。
(1)β-内酰胺酶
它是細菌對 β-内酰胺類抗生素耐藥的(de)主要原因。由于 β-内酰胺酶的(de)産生,使 β-内酰胺類抗生素的(de) β-内酰胺環的(de)酰胺鍵發生斷裂而失去抗菌活性。該類酶可(kě)以爲染色體介導,也(yě)可(kě)爲質粒介導 。
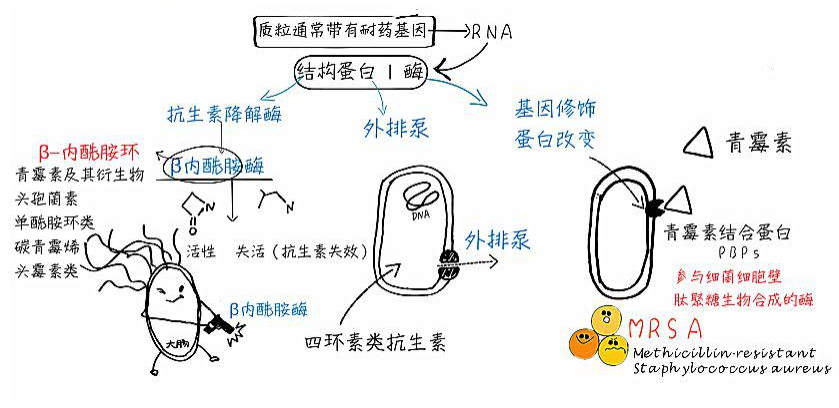
(2)氨基糖苷類鈍化酶
臨床上(shàng)氨基糖苷類耐藥的(de)主要機制(zhì)是鈍化酶的(de)産生,即抗生素的(de)氨基或羟基被酶修飾後與核糖體結合不緊密而不能(néng)進入下一階段發揮抗菌作用(yòng),使細菌在抗生素存在的(de)情況下仍能(néng)存活在細菌胞漿内。
(3)氯黴素乙酰轉移酶
氯黴素乙酰轉移酶是由某些金(jīn)黃(huáng)色葡萄球菌、表皮葡萄球菌、D 組鏈球菌和(hé)革蘭陰性杆菌産生的(de),是一種胞内酶,可(kě)以由染色體、質粒或轉座子基因編碼,使氯黴素轉化爲無抗菌活性的(de)代謝物(wù)。
(4)紅黴素酯化酶
由質粒介導的(de)一種酶,主要作用(yòng)是水(shuǐ)解紅黴素及大(dà)環内酯類抗生素結構中的(de)内酯而使之失去抗菌活性[1]。
2. 藥物(wù)作用(yòng)靶位的(de)變化
耐藥菌藥物(wù)作用(yòng)點的(de)結構或位置發生變化,使藥物(wù)與細菌不能(néng)結合而喪失抗菌效能(néng),或抗生素作用(yòng)的(de)靶位被細菌産生的(de)某種酶修飾或發生突變而使抗菌藥物(wù)無法發揮作用(yòng)。
這種耐藥機制(zhì)在細菌耐藥中普遍存在,作用(yòng)靶位的(de)細微變化都(dōu)有(yǒu)可(kě)能(néng)産生很強的(de)耐藥性。常見的(de)有(yǒu)青黴素結合蛋白(PBP)的(de)改變導緻的(de) β-内酰胺類抗菌藥物(wù)耐藥,MRSA 的(de)産生及 DNA 拓撲異構酶的(de)改變引起喹諾酮類抗菌藥物(wù)耐藥。
3. 滲透屏障通透性改變
由于細菌細胞壁的(de)障礙或細胞膜通透性的(de)改變,使抗生素無法進入細胞内與作用(yòng)靶位結合發揮抗菌效能(néng), 這是細菌的(de)一種非特異性的(de)防衛機制(zhì),主要見于革蘭氏陰性菌。
因爲革蘭陰性菌的(de)外膜同時是疏水(shuǐ)性和(hé)親水(shuǐ)性物(wù)質的(de)屏障。爲了克服這種滲透性障礙,這些微生物(wù)進化出了毛細孔蛋白,在抗生素和(hé)其他(tā)小(xiǎo)分(fēn)子有(yǒu)機化學物(wù)質中充當非特異性的(de)出入口點。當這些毛細孔蛋白數目明(míng)顯減少(shǎo)時,細菌産生耐藥性。
如(rú)銅綠(lǜ)假單胞菌對多種抗菌藥物(wù)的(de)耐藥是因爲其外膜存在著(zhe)獨特的(de)外排系統,其次由于其外膜蛋白 OprF 缺失,使藥物(wù)不易通過所緻。
4. 藥物(wù)主動外排系統
通過主動外排作用(yòng),将藥物(wù)排出菌體外,藥物(wù)的(de)主動外排系統被認爲是導緻細菌對多種抗生素産生耐藥性的(de)重要原因。
目前主要有(yǒu)兩大(dà)類外排系統:特異性外排系統和(hé)多種藥物(wù)耐藥性外排系統。特異性外排系統一般隻作用(yòng)于單一的(de)底物(wù)(藥物(wù)),常常是某一類的(de)抗生素,如(rú)四環素、氯黴素等;而多種藥物(wù)耐藥性外排系統可(kě)以作用(yòng)于多種抗生素或者一些結構和(hé)功能(néng)不相(xiàng)關的(de)複合物(wù)。
5. 其他(tā)
如(rú)細菌通過增加抗菌藥物(wù)的(de)拮抗物(wù)、細菌代謝途徑改變、營養缺陷以及外界環境變化等都(dōu)可(kě)使細菌耐藥性增強。
而且,需要注意的(de)是,細菌耐藥性複雜,臨床上(shàng)很多病原菌同時存在兩種以上(shàng)的(de)耐藥機制(zhì),使之對多種抗菌藥物(wù)同時耐藥。
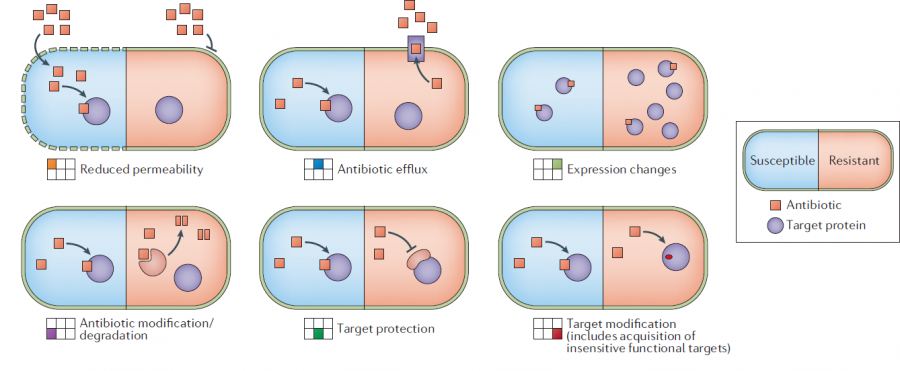
常見的(de)耐藥性産生機制(zhì)[2]



主要抑菌抗生素的(de)作用(yòng)和(hé)常見耐藥機制(zhì)[3]
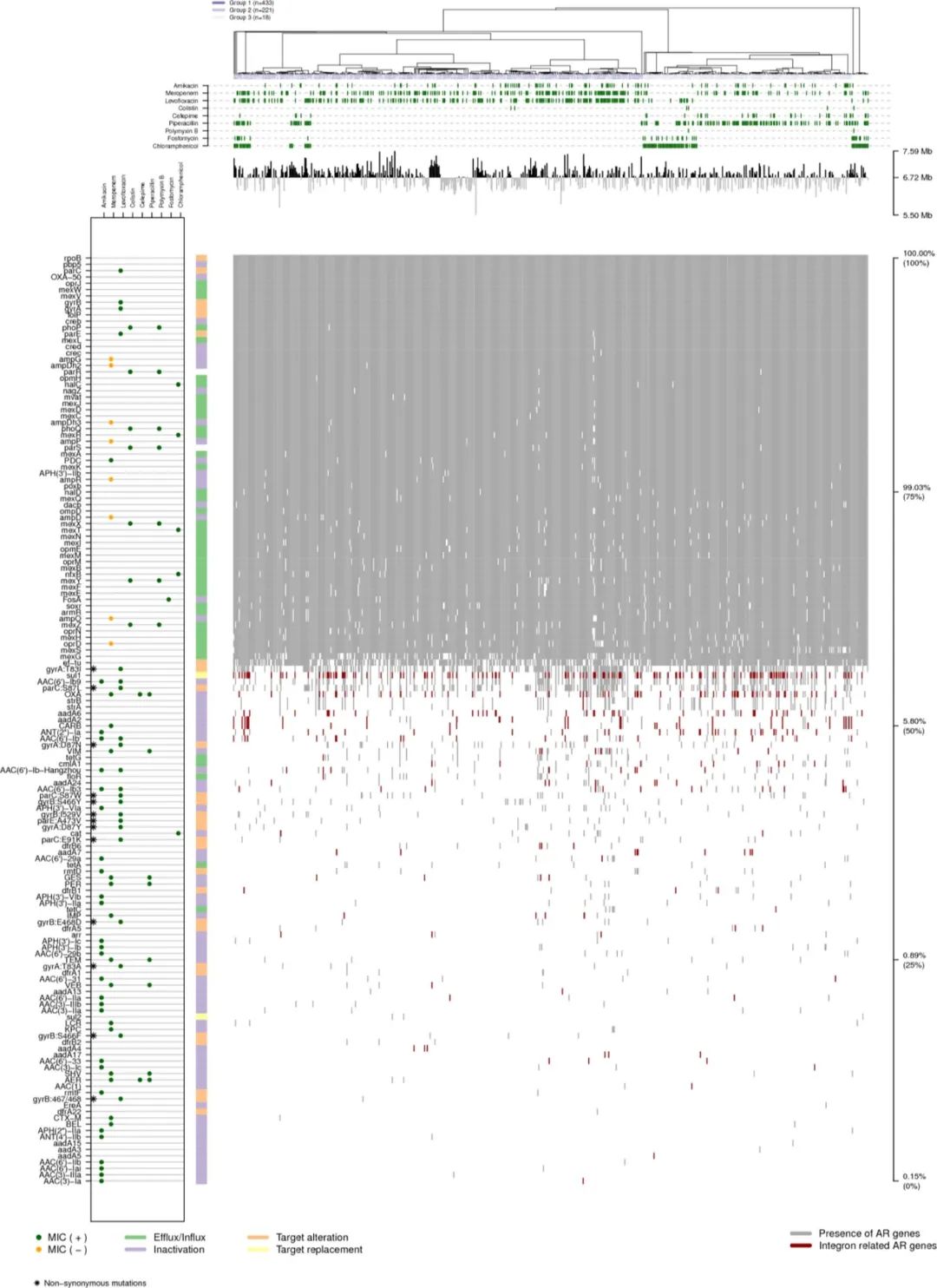
在一項對 672 株銅綠(lǜ)假單胞菌進行(xíng)了基因組序列分(fēn)析的(de)研究發現[4],147 個(gè)緻耐藥因子涵蓋了 5 種耐藥機制(zhì),包括固有(yǒu)和(hé)獲得性耐藥。其中,與藥物(wù)外排和(hé)孔蛋白相(xiàng)關的(de)耐藥性主要是固有(yǒu)的(de),而與抗生素失活相(xiàng)關的(de)耐藥性是獲得性的(de)。
美(měi)格醫學助力臨床精準診斷:
(1)宏基因組二代測序
mNGS 項目檢測範圍基于能(néng)提供廣域搜索、并持續更新的(de)參考基因組數據庫,包含約有(yǒu) 60萬+ 株微生物(wù)參考基因組,檢測展示的(de)結果主要來源于經過細緻整理(lǐ)、可(kě)精确鑒定的(de)微生物(wù)種類數據庫,總共 23796 種。

圖:mNGS 檢測範圍
(2)多重靶向測序 tNGS
tNGS 是 mNGS 技術(shù)的(de)補充,解決了 mNGS 受人(rén)源基因組及背景菌基因組幹擾的(de)問題;解決了 mNGS 對結核、真菌、胞内菌等檢出率低的(de)問題;解決了 mNGS 檢測技術(shù)對 RNA 病毒檢測難度大(dà)的(de)問題;解決了 mNGS 對耐藥基因及毒力因子基因檢測難點的(de)問題。

圖:tNGS 檢測範圍
參考文(wén)獻:
[1] 任豔. 細菌耐藥性産生機制(zhì)及防控措施. 養禽與禽病防治, 2015(05): 2-3.
[2] Manish B, Alaric W. D'S, Gautam D, et al. Sequencing-based methods and resources to study antimicrobial resistance. Nat Rev Genet, 2019, 20(6): 356–370.
[3] Chowdhury M.H, Debprasad D, An N.T.N. Revisiting Antibiotic Resistance: Mechanistic Foundations to Evolutionary Outlook. Antibiotics, 2021, 1(40): 1-23.
[4] Magali J, Alex van B, Kyle C.C, et al. Correlation between phenotypic antibiotic susceptibility and the resistome in Pseudomonas aeruginosa. International Journal of Antimicrobial Agents, 2017, 50(2): 210-218.